肿瘤微环境的复杂性和异质性是导致抗癌药物研发失败率高、临床疗效难以预测的关键原因。尽管3D生物打印等技术为体外肿瘤模型的构建带来了革命性突破,但传统模型往往难以同时实现高细胞密度、仿生血管网络以及可灌注的宏观组织架构,这严重限制了对药物动态渗透、免疫细胞浸润等关键过程的体外模拟。
针对上述挑战,清华大学机械系孙伟教授、庞媛副研究员课题组在 Trends in Biotechnology 期刊上发表了一项题为"Organoid bioprinting for vascularized tumor assembloids"的研究。研究团队提出了一种名为“血管化肿瘤组装体(Vascularized Tumor Assembloids, VTASs)”的新型体外模型构建策略。该策略通过创新的类器官生物打印(Organoid Bioprinting)技术,将内皮化的肝肿瘤聚集体与悬浮内皮细胞整合在水凝胶中,成功构建了具有致密、立体、分层结构且拥有功能性微血管网络的仿生肝肿瘤模型。
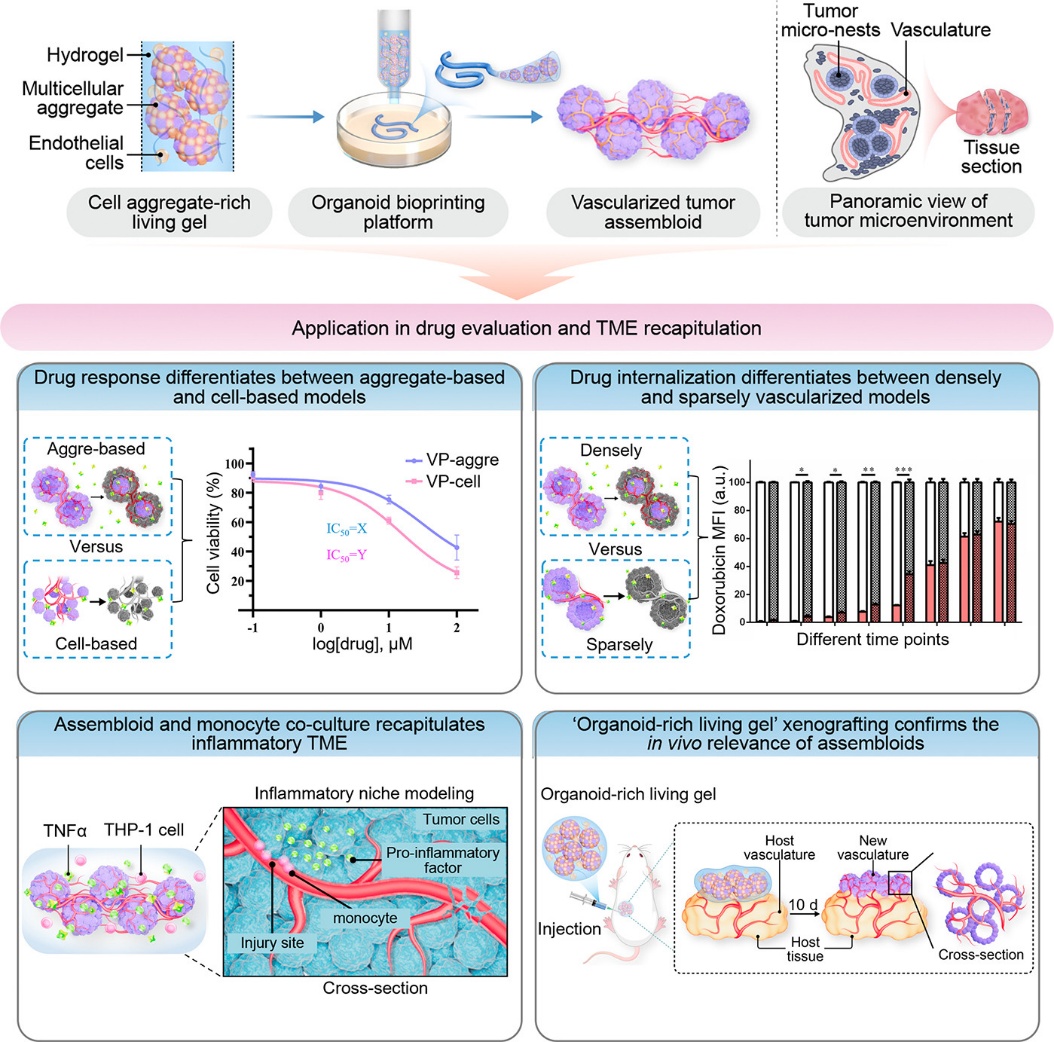
图1:基于类器官生物打印的血管化肿瘤组装体(VTASs)构建策略及其在药物筛选和免疫评估中的应用示意图
在这一类器官打印策略中,研究团队首先通过氧通透性微孔阵列培养装置制备了内皮化的肿瘤细胞聚集体,将其作为模块化“bio-bricks”与悬浮内皮细胞混合,形成富含细胞聚集物的生物墨水。通过挤出式3D生物打印,该墨水被精确沉积为具有宏观尺度的三维结构。培养过程中,这些“bio-bricks”自发融合、重构,最终形成了高细胞密度且内部预置微血管网络结构的立体组织。
在药物筛选应用中,VTASs展现出对临床药物的差异化响应。与传统的单细胞模型或血管稀疏模型相比,具备致密微血管结构的VTASs中细胞凋亡显著减少,且细胞内药物积累出现明显延迟。针对顺铂、索拉非尼、联合治疗以及阿霉素等药物,VTASs均呈现出与体内情况更为接近的反应特征。更重要的是,得益于类器官打印所赋予的仿生微血管结构,研究团队进一步将VTASs与免疫细胞(THP-1单核细胞)共培养,成功模拟了炎症刺激下单核细胞与内皮细胞的相互作用,为研究肿瘤-免疫-血管互作提供了新的体外平台。
在体内植入实验中,VTASs形成了具有灌注功能的类肿瘤结构,并再现了人源肿瘤的关键组织学与生物学特征。这一结果表明,通过预先在体外构建“微血管生态位”, VTASs能够与宿主血管系统快速整合,形成具有灌注功能的类肿瘤组织,体现了类器官打印技术在构建功能性血管网络方面的优势。
清华大学机械系庞媛副研究员为论文通讯作者(兼共同第一作者),清华大学机械系博士研究生周珍珍为共同第一作者。相关研究获得国家自然科学基金、北京市科技计划、国家重点研发计划等项目的支持。
论文链接:
https://www.sciencedirect.com/science/article/pii/S0167779926001447?dgcid=author
https://doi.org/10.1016/j.tibtech.2026.04.009